肝胆类药及消炎类
注射用头孢噻肟钠 更新时间:2018-12-07 17:45:08
【药品名称】
通用名称:注射用头孢噻肟钠
英文名称:Cefotaxime Sodium for Injection
汉语拼音:Zhusheyong Toubaosaiwona
【成份】
本品主要成份为头孢噻肟钠。
化学名称:(6R,7R)-3-[(乙酰氧基)甲基]-7-[2-(2-氨基噻唑-4-基)-2-(甲氧亚氨基)乙酰氨基]-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛-2-烯-2-甲酸钠盐。
化学结构式:
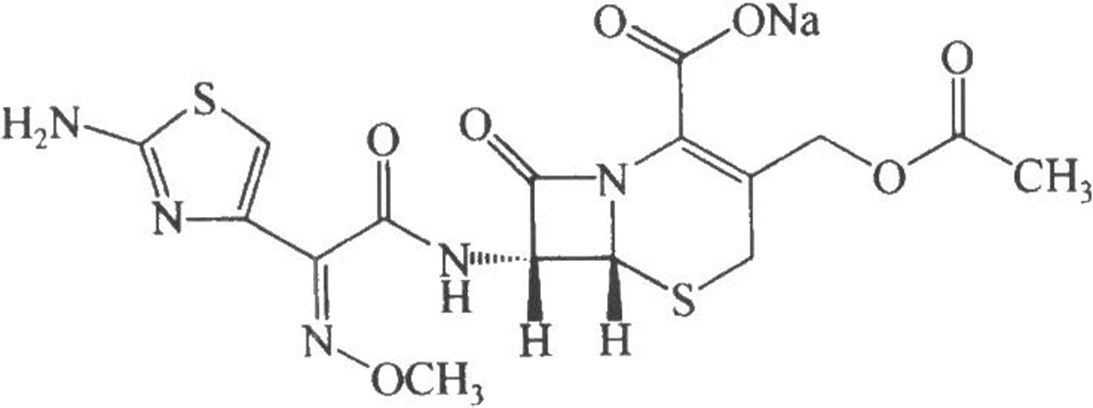
分子式:C16H16N5NaO7S2
分子量:477.45
【性状】
本品为白色至微黄色结晶或粉末。
【适应症】
为减少耐药菌的产生,保证头孢噻肟钠及其他抗菌药物的有效性,头孢噻肟钠只用于治疗或预防已证明或高度怀疑由敏感细菌引起的感染。在选择或修改抗菌药物治疗方案时,应考虑细菌培养和药敏试验结果。如果没有这些试验的数据做参考,则应当根据当地流行病学和病原菌敏感性进行经验性治疗。
在治疗前应进行细菌培养和药敏试验以分离并鉴定感染病原菌,确定其对该抗菌药物的敏感性,在获得以上药敏结果之前可以先使用该抗菌药物进行治疗,得到药敏结果后再选择进行针对病原菌的治疗。
在治疗期间应定期进行细菌培养和药敏试验以掌握病原菌是否对抗菌药物持续敏感,并在细菌出现耐药性后能够及时发现。
本品适用于敏感细菌所致的下列感染:
(1)下呼吸道感染:由肺炎链球菌(原肺炎双球菌)、化脓性链球菌*(A组溶血性链球菌)和其他链球菌(除了肠球菌,如粪肠球菌)、金黄色葡萄球菌(产青霉素酶和不产青霉素酶)、大肠埃希菌、克雷伯菌属 、流感嗜血杆菌(包括氨苄西林耐药菌株)、副流感嗜血杆菌、奇异变形杆菌、黏质沙雷氏菌*、肠杆菌、吲哚阳性变形杆菌属和假单胞菌属(包括铜绿假单胞菌)引起的包括肺炎在内的下呼吸道感染。
(2)泌尿生殖道感染:由肠球菌、表皮葡萄球菌、金黄色葡萄球菌*(产青霉素酶和不产青霉素酶)、枸橼酸杆菌属、肠杆菌属、埃希氏杆菌属、克雷伯菌属、奇异变形杆菌、普通变形杆菌*、斯氏普罗威登菌、摩根氏菌* 、雷氏普罗威登斯菌*、黏质沙雷氏菌和假单胞菌属(包括铜绿假单胞菌)引起的尿路感染。
本品可用于治疗由淋病奈瑟氏菌(包括产青霉素酶菌株)引起的单纯性尿道炎、子宫颈和直肠感染。
(3)妇科感染:由表皮葡萄球菌、链球菌属、肠球菌、肠杆菌属*、克雷伯氏菌属*、大肠埃希菌、奇异变形杆菌、拟杆菌属(包括脆弱拟杆菌*)、梭菌属、厌氧球菌属(包括消化链球菌属和消化球菌属)和梭杆菌属(包括核梭杆菌*)引起的包括盆腔炎、子宫内膜炎和盆腔蜂窝织炎在内的妇科感染。
(4)菌血症/败血症:由大肠埃希菌、克雷伯菌属、粘质沙雷氏菌、金黄色葡萄球菌和链球菌(包括肺炎链球菌)引起的菌血症/败血症。
(5)皮肤及皮肤软组织感染:由金黄色葡萄球菌(产青霉素酶和不产青霉素酶)、表皮葡萄球菌、化脓性链球菌(A组溶血性链球菌)和其他链球菌、肠球菌属、不动杆菌属*、大肠埃希菌、枸橼酸杆菌属(包括弗劳德枸橼酸杆菌*)、肠杆菌属、克雷伯菌属、奇异变形杆菌、普通变形杆菌*、摩根氏菌、雷氏普罗威登斯菌*、假单胞菌属、粘质沙雷氏菌、拟杆菌属和厌氧球菌属(包括消化链球菌属和消化球菌属)引起的皮肤及皮肤软组织感染。
(6)腹腔感染:由链球菌属*、大肠埃希菌、克雷伯菌属、拟杆菌属、厌氧球菌属(包括消化链球菌属*和消化球菌属*)、奇异变形杆菌*和梭菌属*引起的包括腹膜炎在内的腹腔感染。
(7)骨和关节感染:由金黄色葡萄球菌(产青霉素酶和不产青霉素酶)、链球菌属(包括化脓性链球菌*)、假单胞菌属(包括铜绿假单胞菌*)和奇异变形杆菌*引起骨和关节感染。
(8)中枢神经系统感染:由脑膜炎奈瑟氏菌、流感嗜血杆菌、肺炎链球菌、克雷伯菌属*和大肠埃希菌*引起的中枢神经系统感染,例如脑膜炎和脑室炎。
(*)在人体器官系统中,这种微生物的有效性研究少于10例感染。
【规格】
按C16H17N5O7S2计(1)1.0g (2)2.0g
【用法用量】
一、成人及12岁以上儿童
一般感染:一次1g,每日2次,肌内或静脉注射。
中度感染:一次2g,每日2次,肌内或静脉注射或静脉滴注。
严重感染:一次2~4g,每8~12小时一次,静脉注射或静脉滴注,每日剂量不超过12g。
淋病:0.5~1g肌内注射(单次给药已足)。
二、12岁及以下儿童
一般感染:50~100mg/kg/日间隔6~12小时等剂量分次静脉注射或静脉滴注。
严重感染:150~200mg/kg/日分次静脉注射。
7天内新生儿每12小时1次。7~28天新生儿每8小时1次,每次剂量均为25mg/kg。早产儿每日剂量不可超过50mg/kg。
三、预防感染
外科大手术麻醉前0.5~1小时1g肌内或静脉注射,术中1g,术后每6~8小时1g,至24小时内为止。
四、严重肾功能减退病人应用本品时须适当减量。
血清肌酐值超过424μmol/L(4.8mg)或肌酐清除率低于20ml/分钟时,头孢噻肟的维持量应减半;血清肌酐值超过751μmol/L(8.5mg)时,维持量为正常量的1/4。需血液透析者每日0.5~2g。但在透析后应加用1次剂量。
配制方法:
- 肌内注射:本品1g溶于4ml 1%或2%利多卡因注射液中,深层肌内注射,可避免疼痛;或溶于4ml灭菌注射用水中,深层肌内注射。剂量超过2g时,应分不同部位注射。
- 静脉注射:本品1g溶于10ml以上灭菌注射用水,经5~10分钟缓慢静脉注射。本品2g溶于40ml的灭菌注射用水中或40ml 10%葡萄糖注射液中于20分钟内缓慢静脉注射。
- 静脉滴注:本品2g溶于40ml的灭菌注射用水中或40ml 10%葡萄糖注射液中于20分钟内注射完,也可溶于100ml等渗液中或10%葡萄糖注射液中于40~60分钟内静脉滴注完。
1g本品溶于14ml灭菌注射用水时形成等渗溶液。
【不良反应】
临床试验:
本品通常耐受性良好,头孢噻肟最常见的不良反应是在肌内或静脉注射后发生的局部反应,其他不良反应很少发生。
最常发生的不良反应(发生率>1%)为:
局部反应(4.3%):静脉注射后注射部位炎症反应,肌内注射后的疼痛、硬化和压痛。
过敏反应(2.4%):皮疹、瘙痒症、发热、嗜酸性粒细胞增多。
胃肠道反应(1.4%):结肠炎、腹泻、恶心和呕吐。
不常发生的不良反应(发生率<1%)为:
血液系统紊乱:粒细胞生成障碍、白细胞减少。
泌尿生殖系统:念珠菌病、阴道炎。
中枢神经系统:头痛。
实验室检查:AST、ALT、LDH、ALP和BUN的暂时性升高,有些患者会出现直接Coombs试验阳性。
上市后经验:
在批准上市后使用头孢噻肟注射剂,已经报道了下列的不良反应。由于这些不良反应来自不确定人群量的自发性报道,因此不能可靠地估计这些不良反应的发生频率和/或确定其与药物暴露之间的因果关系。
心血管系统:已有报道通过中心静脉导管进行快速(<60s)大剂量注射给药发生潜在威胁生命的心律失常。
中枢神经系统:对特别是肾功能损害的患者进行包括头孢噻肟在内的β-内酰胺类抗生素高剂量给药,可能会导致脑病(如:意识障碍,动作异常和抽搐)。头晕也有报道。
皮肤:同其他头孢菌素类抗生素一样,有报道本品出现中毒性表皮坏死松解症,Stevens-Johnson综合征和多形性红斑的个案。也有报道使用头孢噻肟钠治疗引起急性全身泛发性发疹性脓疱症(AGEP)的病例。
注射部位状况:注射部位的炎症反应,包括静脉炎/血栓性静脉炎。
血液系统:溶血性贫血、粒细胞缺乏症、血小板减少症、血细胞减少症、骨髓抑制。
过敏反应:全身过敏性反应(如全身过敏反应、支气管痉挛、过敏性休克),荨麻疹。
肾脏:间质性肾炎、血清肌酐值暂时升高、急性肾功能衰竭。
肝脏:肝炎、黄疸、胆汁淤积、γ-GT和胆红素升高。
头孢菌素类药物不良反应
除了上述不良反应外,头孢噻肟钠在使用过程中还有下列头孢菌素类抗生素不良反应的报道:过敏反应、肝功能受损(包括胆汁淤积)、再生障碍性贫血、出血。
有些头孢菌素类药物与引发癫痫有关,特别是对于没有减少用药剂量的肾功能减退患者。当治疗期间发生癫痫,应停止用药,根据临床需要采取抗惊厥治疗。
【禁忌】
对头孢菌素过敏者及有青霉素过敏性休克或即刻反应史者禁用本品。
【注意事项】
1.交叉过敏反应:对一种头孢菌素或头霉素过敏者对其他头孢菌素或头霉素也可能过敏。对青霉素或青霉胺过敏者也可能对本品过敏。用药前应详细询问过敏史,本品需进行过敏试验。
2.对诊断的干扰:应用本品的病人抗球蛋白(Coombs)试验可出现阳性反应;孕妇产前应用本品,此反应可出现于新生儿。用硫酸铜法测定尿糖可呈假阳性。血清碱性磷酸酶、血尿素氮、丙氨酸氨基转移酶、天门冬氨酸氨基转移酶或血清乳酸脱氢酶值可增高。
3有胃肠道疾病史,特别是结肠炎者应慎用本品。应用头孢噻肟可能引起假膜性肠炎。在应用过程中如发生腹泻且怀疑为假膜性肠炎时,应立即停药并予以甲硝唑口服,无效时考虑口服万古霉素和去甲万古霉素。
4.肾功能减退患者应用本品时需要根据患者的肾功能、病原体的敏感性及感染的严重程度调整剂量。肌酐清除率小于20ml/min者,给药剂量应减半。
5.本品与氨基糖苷类不可同瓶滴注。
6.长期应用本品可能导致不敏感菌或耐药菌的过度繁殖,需要严密观察,一旦发生二重感染,需进行相应处理。
7.应用本品治疗可能发生中性粒细胞较少及罕见的粒细胞缺乏症,尤其是长期治疗。因此,疗程超过10日者应监测血常规。
8.本品对局部组织有刺激作用。在绝大多数病例中,改变注射部位即可解决血管周围外渗。极个别情况下可能发生广泛血管周围外渗,并导致组织坏死,可能需要外科治疗。
9.当治疗盆腔炎患者,疑似病原体之一为沙眼衣原体时,需联合应用抗衣原体药物进行治疗。
【孕妇及哺乳期妇女用药】
本品可经乳汁排出,哺乳期妇女应用本品时虽无发生问题的报告,但应用本品时宜暂停哺乳。本品可透过血胎盘屏障进入胎儿血循环,孕妇应限用于有确切适应症的患者,权衡利弊后使用。
【儿童用药】
儿童仅适用于静脉给药,并应密切观察是否出现液体外渗,具体参见【用法用量】。
【老年用药】
老年患者用药根据肾功能适当减量。
本品主要通过肾脏排泄,对于肾功能受损的患者来说,使用本品出现毒性的风险更大。因为老年患者更容易发生肾功能减退,应谨慎选择给药剂量,同时密切监测肾功能(参见【注意事项】部分)。
【药物相互作用】
1.与庆大霉素或妥布霉素合用对铜绿假单胞菌均有协同作用;与阿米卡星合用对大肠杆菌、肺炎克雷伯菌和铜绿假单胞菌有协同作用,对金葡菌无此作用。
2.与氨基糖苷类抗生素联合应用时,应分瓶给药,不能混在同一容器中,用药期间应随访肾功能。
3.大剂量头孢噻肟与强利尿药联合应用时,应注意肾功能变化。
4.头孢噻肟可用氯化钠注射液或葡萄糖注射液稀释,但不能与碳酸氢钠液混合。
5.与阿洛西林或美洛西林等合用,可使本品的总清除率降低,如两者合用需适当减低剂量。
6.丙磺舒会干扰肾小管对头孢噻肟的转化,使头孢噻肟的清除率减少大约50%,头孢噻肟的血浓度升高。头孢噻肟给药超过6g/d的患者应避免使用丙磺舒。
【药物过量】
β-内酰胺类过量可能会出现可逆的代谢性脑病(神经紊乱、异常动作、惊厥发作)。本品无特效拮抗药,药物过量时主要给予对症治疗和大量饮水及补液等。注意本品对肝肾功能造成的影响。
【药理毒理】
药理作用
作用机制
头孢噻肟为第三代头孢菌素,其作用机制为抑制细菌细胞壁合成。
抗菌活性
头孢噻肟在某些β-内酰胺酶(青霉素酶和头孢菌素类酶)存在下,对革兰阳性菌和革兰阴性菌均有抗菌活性。
在体外试验及【适应症】项下的临床感染中,头孢噻肟已被证实对以下微生物的大部分菌株具有抗菌活性。
革兰阳性菌
肠球菌属1
金黄色葡萄球菌(仅甲氧西林敏感菌菌株)
表皮葡萄球菌
肺炎链球菌
化脓性链球菌(A组 β-溶血性链球菌)
链球菌属(草绿色链球菌)
革兰阴性菌
不动杆菌属
枸橼酸杆菌属2
肠杆菌属2
大肠埃希菌2
流感嗜血杆菌
副流感嗜血杆菌
克雷伯菌属(包括肺炎克雷伯菌)2
摩根氏菌2
淋病奈瑟氏球菌(包括β-内酰胺酶阳性和阴性菌株)
脑膜炎奈瑟氏菌
奇异变形杆菌2
普通变形杆菌2
雷氏普罗威登斯菌2
斯氏普罗威登菌2
粘质沙雷氏菌2
1肠球菌可能对头孢噻肟具固有耐药性。
2绝大多数产超广谱β-内酰胺酶(ESBL)及产碳青霉烯酶的分离菌株对头孢噻肟耐药。
厌氧菌
拟杆菌属,包括一些脆弱拟杆菌属。
梭菌属(大多数艰难梭菌分离菌株是抗性的)
梭菌属(包括核梭菌杆菌)
消化球菌
消化链球菌属
以下的体外数据是可用的,但是其临床意义尚未明确。至少90%以下的微生物体外最小抑菌浓度(MIC)小于或等于1μg/ml。然而,尚未具有充分的依据和良好控制的临床试验证明头孢噻肟对以下微生物引起的临床感染的有效性。
革兰阴性菌
普罗维登斯菌属
沙门氏菌属(包括伤寒杆菌)
志贺氏菌属
耐药机制
细菌耐药机制主要通过β-内酰胺酶的水解作用、青霉素结合蛋白(PBPs)的改变及膜通透性下降。
药敏试验
细菌对头孢噻肟的敏感性存在地理差异性,可能随时间发生变化;如果允许的话,临床微生物实验室应该为使用抗菌药物的住院医生提供由医院或社区获得的病原体的体外药敏试验的阶段性报告。这些报告将有助于医生选择何种抗菌药物进行治疗。
稀释法
采用定量方法测定最小抑菌浓度(MICs),这些最小抑菌浓度值可用于评估细菌对抗菌药物的敏感程度。应采用标准测试方法(肉汤法或琼脂法)来测定MICs,可根据表1中的标准对测定的MICs值进行解释。
扩散法
采用对抑菌圈直径进行测定的定量方法,同样可对细菌对抗微生物化合物的敏感性进行可重复性估计。抑菌圈的大小代表着细菌对抗菌药物敏感程度,应采用标准测试方法进行测定。该法使用浸渍着30μg的头孢噻肟的纸片对细菌对抗菌药物的敏感程度进行测定,纸片扩散情况依据表1中的标准进行判定。
厌氧技术
对于厌氧菌,头孢噻肟药敏试验最小抑菌浓度(MICs)可通过标准琼脂扩散法检测。获得的最小抑菌数值应该按表1中的标准进行判定。
表1:头孢噻肟敏感性试验判定标准
| 病原体 |
最小的抑菌浓度(μg/ml) |
抑菌直径(mm) |
| 敏感(S) |
中介(I) |
耐药(R) |
敏感(S) |
中介(I) |
耐药(R) |
| 不动杆菌属 |
≤1 |
2 |
≥4 |
- |
- |
- |
| 肠杆菌 |
≤1 |
2 |
≥4 |
≥26 |
23-25 |
≤22 |
| 嗜血杆菌属*† |
≤1 |
- |
- |
- |
- |
- |
| 淋病奈瑟氏菌* |
≤0.5 |
- |
- |
≥31 |
- |
- |
| 脑膜炎奈瑟氏菌* |
≤0.12 |
- |
- |
≥34 |
- |
- |
肺炎链球菌‡
脑膜炎菌属 |
≤0.5 |
1 |
≥2 |
- |
- |
- |
肺炎链球菌‡
非脑膜炎菌属 |
≤1 |
2 |
≥4 |
- |
- |
- |
链球菌属
β-溶血性族* |
≤0.5 |
- |
- |
≥24 |
- |
- |
| 草绿色链球菌属 |
≤1 |
2 |
≥4 |
≥28 |
26-27 |
≤25 |
| 其他非肠杆菌⋚ |
≤1 |
2 |
≥4 |
- |
- |
- |
| 厌氧菌(琼脂法) |
≤1 |
2 |
≥4 |
- |
- |
- |
敏感折点是基于肾功能正常患者每8小时1g的单次给药。
葡萄球菌对头孢噻肟的敏感性可能从青霉素和头孢西丁/苯唑西林的测试中推测得出。
*当前缺乏耐药菌株除“敏感”类别项以外的其他数据。若耐药菌株MIC值的结果与敏感不一致,则应在参比实验室中进行额外的测试。
†嗜血杆菌属只包括流感嗜血杆菌和副流感嗜血杆菌。
‡纸片扩散法的解释标准不适用于头孢噻肟平皿测定肺炎链球菌的敏感性,但是,肺炎双球菌株对苯唑西林的抑菌直径大于20mm时,可以认为是对青霉素是敏感的(MIC≤0.06μg/ml),同样可以认为是对头孢噻肟是敏感的。不能仅依据苯唑西林抑菌圈直径≤19mm,就判定肺炎链球菌对青霉素(头孢噻肟)耐药或是中介。头孢噻肟的MIC应由苯唑西林对那些抑菌直径≤19mm的菌株所决定。
⋚“敏感”报道表明,如果当杀菌剂在感染部位达到有效浓度,病原体很大程度上会被抑制生长。“中介”报道表明,该结果是不明确的,如果微生物对可替换的临床可行药物不完全敏感,则应重复进行该测试。这个分类意味着在药物生理性聚集的身体部位或在能使用高剂量的情况下可能的临床适用性。这个分类还能提供一个缓冲空间来防止小的、不受控制的技术因素导致的解释差异。“耐药”报道表明,如果杀菌剂在感染部位能达到有效浓度而很大程度不能抑制病原体的生长的,则应该采取其他的治疗方法。
质量控制
标准化药敏试验过程要求利用实验室监控并确保测定过程中供试品和分析试剂的准确度和精密度,以及个人操作实验的技术水平。应提供具有表2中MIC值的头孢噻肟粉末标准品。对于使用扩散法的30μg的头孢噻肟纸片的抑菌直径标准应该符合表2的数值。
表2:头孢噻肟可接受的质控标准
| 质量控制种类 |
最小抑菌浓度(μg/ml) |
抑菌直径(mm) |
| 大肠埃希菌ATCC 25922 |
0.03-0.12 |
29-35 |
| 金黄色葡萄球菌ATCC 29213 |
1-4 |
- |
| 金黄色葡萄球菌 ATCC 25923 |
- |
25-31 |
| 铜绿假单胞菌 ATCC 27853 |
8-23 |
18-22 |
| 流感嗜血杆菌AYCC 49247 |
0.12-0.5 |
31-39 |
| 肺炎链球菌ATCC 49619 |
0.03-0.12 |
31-39 |
| 淋病奈瑟氏菌ATCC 49226 |
0.015-0.06 |
38-48 |
| 脆弱拟杆菌*ATCC 25285 |
8-32 |
- |
| 多形拟杆菌*ATCC 29741 |
16-64 |
- |
| 兰特真菌ATCC 43055 |
64-256 |
- |
*参照琼脂稀释方法。
毒理研究
遗传毒性
头孢噻肟在小鼠微核试验和细菌回复突变试验中未见致突变作用。
生殖毒性
大鼠皮下给药高达250mg/kg/日(基于mg/m2,0.2倍最大人用剂量)或小鼠静脉注射2000mg/kg/日(基于mg/m2,0.7倍人用剂量)时,头孢噻肟对其生育力不造成损害。
妊娠小鼠静注1200mg/kg/日(基于mg/m2,0.4倍人用剂量)或妊娠大鼠静注1200mg/kg/日(基于mg/m2,0.8倍人用剂量)的生殖毒性研究中,未见胚胎毒性和致畸性。
大鼠围产期和产后的生殖毒性研究中,21天哺乳期内头孢噻肟1200mg/kg/日给药组大鼠幼仔出生体重明显减轻,幼仔生长速度缓慢。
致癌性
未进行动物终生研究以评价头孢噻肟的致癌性。
【药代动力学】
肌内注射本品0.5g或1.0g后,0.5小时达血药峰浓度(Cmax),分别为12 mg/L和25 mg/L,8小时后血中仍可测出有效浓度。于5分钟内静脉注射本品1g或2g,即刻血药峰浓度分别为102 mg/L和215 mg/L,4小时后2 g组尚可测得3.3 mg/L。30分钟内静脉滴注1g后的即刻血药浓度为41mg/L,4小时的血药浓度为1.5 mg/L。头孢噻肟广泛分布于全身各种组织和体液中。正常脑脊液中的药物浓度很低,脑膜炎患者应用本品后,脑脊液中可达有效浓度。支气管分泌物、中耳溢液、胸腔积液、脓胸脓液、腹水、胆囊壁、胆汁、骨组织中亦均可达到有效浓度。本品可透过血-胎盘屏障进入胎儿血循环,少量亦可进入乳汁。白内障病人静脉注射2g后,前房液中药物浓度为0.3~2.3mg/L,蛋白结合率30%~50%。1/3~1/2的药物在体内代谢成为去乙酰头孢噻肟(抗菌活性为头孢噻肟的1/10)和其他无活性的代谢物。本品血消除半衰期(t1/2β)为1.5小时,老年人的t1/2β(2~2.5小时)较年轻人为长,肾功能不全者t1/2β可延长为14.6小时。约80%(74%~88%)的给药量经肾排泄,其中约50%~60%为原形药,10%~20%为去乙酰头孢噻肟,头孢噻肟经胆汁排泄的量甚少,约为给药量的0.01%~0.1%。丙磺舒可使头孢噻肟的肾清除率减少5%,t1/2β延长45%。血液透析能将62.3%的药物自体内清除。腹膜透析对药物的清除量很少。
【贮藏】
避光,密闭,不超过25℃保存。
【包装】
中硼硅玻璃管制注射剂瓶、注射用无菌粉末用覆聚四氟乙烯/六氟丙烯的共聚物膜氯化丁基橡胶塞包装。
(1) 1.0g规格:1瓶/盒,10瓶/盒
(2) 2.0g规格:1瓶/盒,10瓶/盒
【有效期】
18个月
【执行标准】国家药品监督管理局药品注册标准YBH05382022
【批准文号】
(1) 1.0g规格:国药准字H20023022
(2) 2.0g规格:国药准字H20033992
